L’acido formico non è davvero piatto: nuovi esperimenti mostrano che gli atomi oscillano nello spazio, rompendo la simmetria e generando chiralità quantistica. Una scoperta che ribalta la chimicatradizionale e rivela la vera natura tridimensionale delle molecole
Molecole in continuo movimento: la prova che la planarità non esiste.
L’acido formico è considerato una molecola in cui tutti gli atomi giacciono su un unico piano. Un gruppo di ricerca della Goethe University, insieme a partner di cooperazione, ha ora dimostrato sperimentalmente che gli atomi dell’acido formico oscillano continuamente fuori da questo piano su una scala minima. Di conseguenza, la molecola non è per la maggior parte del tempo piatta, ma tridimensionale, perdendo così la sua simmetria. Il tremolio degli atomi è un effetto della fisica quantistica, secondo cui le particelle non sono mai completamente a riposo.
I tradizionali libri di chimica presentano un quadro ordinato: gli atomi nelle molecole occupano posizioni fisse, collegati da aste rigide. Una molecola come l’acido formico (acido metanoico, HCOOH) viene immaginata come bidimensionale - piatta come un foglio di carta. Ma la fisica quantistica racconta un’altra storia. In realtà, la natura resiste alla rigidità e costringe anche le strutture più semplici nella terza dimensione.
I ricercatori guidati dal professor Reinhard Dörner (1) dell’Istituto di Fisica Nucleare della Goethe University Frankfurt hanno ora determinato la struttura spaziale precisa della molecola di acido formico “piatta” utilizzando un fascio di raggi X proveniente dalla sorgente di radiazione di sincrotrone PETRA III presso il centro di accelerazione DESY ad Amburgo. Hanno collaborato con colleghi delle università di Kassel, Marburg e Nevada, del Fritz Haber Institute e del Max Planck Institute for Nuclear Physics.
Per farlo, hanno sfruttato due effetti che si verificano quando la radiazione a raggi X colpisce una molecola. Innanzitutto, la radiazione espelle diversi elettroni dalla molecola (effetto fotoelettrico ed effetto Auger). Di conseguenza, gli atomi diventano così altamente carichi che la molecola esplode in frammenti (Coulomb explosion). Gli scienziati sono riusciti a misurare questi processi in sequenza, nonostante avvengano nell’arco di femtosecondi - milionesimi di miliardesimo di secondo.
A questo scopo, hanno utilizzato un apparato inventato alla Goethe University e continuamente perfezionato da allora: il microscopio a reazione COLTRIMS. Sulla base dei dati di misura, sono poi riusciti a calcolare la geometria originale della molecola di acido formico. Il risultato: i due atomi di idrogeno dell’acido formico oscillano leggermente avanti e indietro, il che significa che la molecola non è piatta.
Il dottor Reinhard Dörner spiega: «Nel mondo quantistico, i nuclei atomici non sono minuscole sfere che rimangono fisse. Assomigliano piuttosto a nuvole vibranti. Anche se raffreddiamo una molecola fino allo zero assoluto, questo tremolio - il cosiddetto moto del punto zero - non si ferma mai».
La conseguenza è radicale: un nucleo atomico non ha una posizione esatta, ma solo una probabilità di trovarsi in un determinato punto. In un certo senso, è “un po’ ovunque”. Di conseguenza, una molecola di acido formico è di fatto tridimensionale in quasi ogni istante.
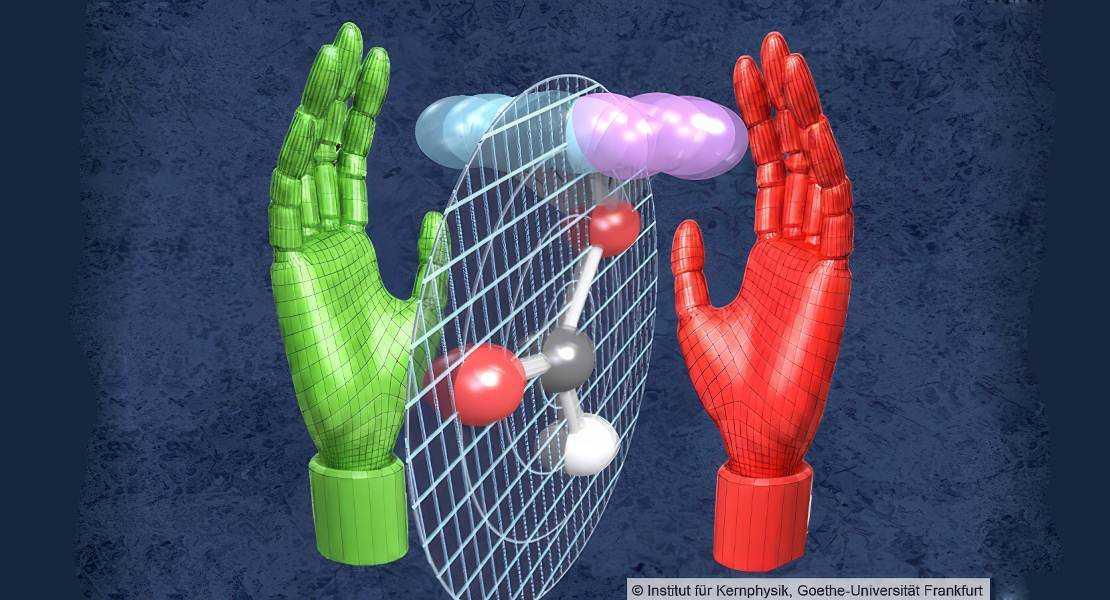
Dörner aggiunge: «Attraverso questo minuscolo passo nella terza dimensione, la molecola perde la sua simmetria e non può più essere sovrapposta alla sua immagine speculare - in modo simile alle nostre mani destra e sinistra. L’acido formico è chirale - ha una forma levogira per metà del tempo e una forma destrogira per l’altra metà».
In chimica, due forme chirali di questo tipo - i cosiddetti enantiomeri - possono avere effetti completamente diversi: mentre una forma di una molecola può agire come un medicinale, la sua immagine speculare può essere inefficace. Normalmente, questa chiralità nasce dalla struttura fissa di una molecola.
Il dottor Dörner conclude: «Come siamo riusciti a mostrare usando l’esempio dell’acido formico, il tremolio quantistico da solo può generare due diverse realtà speculari a partire da una molecola simmetrica. Ciò significa che la chiralità - una proprietà importante della vita - qui non deriva dal progetto statico della molecola, ma unicamente dal tremolio incessante nel mondo quantistico. Più in generale, i nostri risultati con l’acido formico mostrano che la geometria non è una proprietà statica ma un evento dinamico, e che una molecola piatta è in realtà solo il valore medio dei suoi atomi che tremano in tutte le direzioni».
Riferimenti:
(1) Reinhard Dörner
Descrizione foto: La vibrazione del punto zero della meccanica quantistica - il “tremore” degli atomi - rende l’acido formico una molecola chirale le cui due forme, come la mano destra e quella sinistra, non possono essere sovrapposte. - Credit: Institute for Nuclear Physics, Goethe University Frankfur.
Autore traduzione riassuntiva e adattamento linguistico: Edoardo Capuano / Articolo originale: The quantum trembling: Why there are no truly flat molecules